Original source: https://www2.tulane.edu/~wiser/protozoology/notes/api.html
Los apicomplexa son un grupo monofilético compuesto casi en su totalidad por especies parásitas (es decir, no de vida libre). Apicomplexa, junto con ciliados y dinoflagelados, forman un grupo de orden superior conocido como Alveolata. Una característica importante que define a este grupo son las estructuras aplanadas similares a vesículas, llamadas alvéolas corticales, que se encuentran justo debajo de la membrana plasmática. Antiguamente los apicomplexa formaban parte de un grupo llamado esporozoos y este nombre todavía se utiliza en ocasiones. Ha habido algunas sugerencias para volver al nombre esporozoos (Cox, Tr. Parasitol. 18:108 ).
La microscopía electrónica reveló características ultraestructurales únicas entre los diversos esporozoos que posteriormente se utilizaron para redefinir los grupos. Una característica definitoria del apicomplexa es un grupo de orgánulos que se encuentran en un extremo, llamado extremo apical, del organismo. Este ‘complejo apical’ incluye orgánulos secretores conocidos como micronemas y róptrios , anillos polares compuestos de microtúbulos y, en algunas especies, un conoide que se encuentra dentro de los anillos polares. En algún momento durante su ciclo de vida, los miembros del apicomplejo invaden o se adhieren a las células huésped. Es durante esta etapa invasiva (y/o móvil) que se expresan estos orgánulos apicales, así como las membranas subpeliculares, que en realidad son alvéolos corticales. Los orgánulos apicales desempeñan un papel en la interacción del parásito con la célula huésped y la posterior invasión de la célula huésped. (Ver discusión detallada sobre la invasión de las células huésped por el parásito de la malaria). Las formas móviles de apicomplexa se arrastran a lo largo del sustrato de una manera no ameboide conocida como motilidad deslizante. Muchas especies de apicomplejos tienen gametos flagelados .
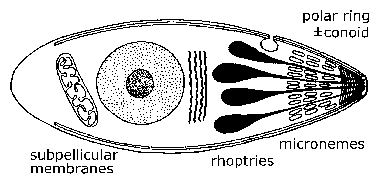 | 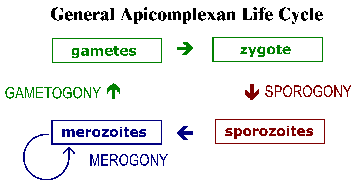 |
| Estructura general y ciclo de vida del apicomplejo . Las formas invasivas y/o móviles de apicomplexa exhiben características ultraestructurales distintivas que pueden observarse con el microscopio electrónico. En el extremo apical hay un anillo de microtúbulos conocido como anillo polar. A veces también se ve una estructura citoesquelética elaborada conocida como conoide. En este extremo también se ven pequeñas vesículas elípticas conocidas como micronemas, así como orgánulos en forma de lágrima llamados rhoptries. | |
Los apicomplexa tienen ciclos de vida complejos que se caracterizan por tres procesos distintos: esporogonia, merogonía y gametogonía (Figura). Aunque la mayoría de los apicomplexa exhiben este ciclo de vida general, los detalles pueden variar entre especies. Además, la terminología utilizada para describir estas diversas etapas del ciclo de vida varía entre las especies. El ciclo de vida consta tanto de formas que se reproducen asexualmente como de etapas sexuales. En especies monoxénicas, estos tres procesos se llevarán a cabo en un solo huésped y, a menudo, en un solo tipo de célula o tejido. Mientras que, en especies heteroxenas, los diversos procesos se llevarán a cabo en diferentes huéspedes y generalmente involucrarán diferentes tejidos.
La esporogonia ocurre inmediatamente después de una fase sexual y consiste en una reproducción asexual que culmina con la producción de esporozoítos. Los esporozoitos son una forma invasiva que invadirá las células y se desarrollará en formas que sufrirán otra replicación asexual conocida como merogonía. La merogonía y los merozoitos resultantes se conocen con muchos nombres diferentes según la especie. A diferencia de la esporogonia, en la que generalmente hay una sola ronda de replicación, con bastante frecuencia hay múltiples rondas de merogonía. En otras palabras, los merozoítos, que también son formas invasivas, pueden volver a invadir las células e iniciar otra ronda de merogonía. A veces, estas múltiples rondas de merogonía implicarán un cambio en el organismo huésped o un cambio en el tipo de célula invadida por el parásito, lo que dará como resultado distintas etapas de merogonía. Como alternativa a la replicación asexual, los merozoitos pueden convertirse en gametos mediante un proceso denominado gametogonía, gamogonía o gametogénesis. Como en otros tipos de reproducción sexual, los gametos se fusionan para formar un cigoto que sufrirá esporogonia.
| PlasmodioBabesiacriptosporidioisósporaciclosporaSarcocististoxoplasma |
Los apicomplexa son un grupo extremadamente grande y diverso (>5000 especies nombradas). Siete especies infectan a los humanos (Cuadro). Plasmodium , como agente causante de la malaria, tiene el mayor impacto en la salud humana. Babesia es una infección zoonótica relativamente rara. Las otras cinco especies están todas clasificadas como coccidios. Sin embargo, datos moleculares recientes indican que Cryptosporidium está más estrechamente relacionado con las gregarinas que con los coccidios. Los coccidios generalmente se consideran patógenos oportunistas y a menudo se asocian con el SIDA. Varios parásitos apicomplejos también son importantes en términos de medicina veterinaria y agricultura. Las más notables son Babesia y Theileria en ganado vacuno y Eimeria en aves de corral.
| Orígenes de las algas del Apicomplexa |
Históricamente, los apicomplexa han sido descritos como un grupo con únicamente formas parásitas. Esto y sus orgánulos apicales únicos plantean preguntas sobre el origen del grupo. El análisis filogenético indica que los miembros del género Copodella forman un grupo hermano con los apicomplexa (1). Los colpodélidos son flagelados depredadores que se alimentan de algas unicelulares mediante un proceso llamado mizocitosis. La mizocitosis implica que el depredador (o parásito) se adhiera a la presa (o huésped) y literalmente succione el citoplasma de la célula de la presa a través de estructuras especializadas. Esta unión e interacción con la célula presa está mediada por orgánulos similares a los que utiliza el apicomplejo para unirse o invadir las células huésped. Por lo tanto, la evolución del apicomplexa probablemente evolucionó desde esta depredación myzocitoica hasta el parasitismo mizocitoico, como lo exhiben las gregarinas y Cryptosporidium , hasta el parasitismo intracelular.Otros organismos mizocitoicos con apicomplexa como orgánulos apicales incluyen Perkinsus , parásito de ostras y almejas, y Parvilucifera , un depredador de dinoflagelados. Estos perkinsidos, sin embargo, forman un grupo hermano con los dinoflagelados y no con los apicomplexa (Figura). Esto sugiere que el progenitor de los clados de dinoflagelados y apicomplejos puede haber sido un flagelado depredador y que los orgánulos apicales se retuvieron en el clado de apicomplejos, pero se perdieron en la mayor parte del clado de dinoflagelados.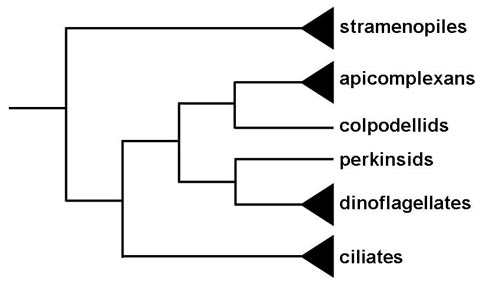 La otra conexión entre las algas y los apicomplejos es un remanente de cloroplasto, llamado apicoplasto, que se encuentra en la mayoría de los apicomplejos (2). El apicoplasto es probablemente el resultado de una endosimbiosis secundaria de un alga roja y probablemente sea el mismo evento endosimbiótico que da lugar a los plastidios de los dinoflagelados. El apicoplasto no es fotosintético, pero exhibe actividades asociadas con la biosíntesis de ácidos grasos tipo II, la biosíntesis de isoprenoides y posiblemente la síntesis de hemo. Estas vías son esencialmente procarióticas y representan excelentes objetivos farmacológicos. También se ha identificado un alveolado fotosintético, Chromera velia , que parece ser el apicomplejo de ramificación más temprana (3).Kuvardina, ON, BS Leander, VV Aleshin, AP Myl’nikov, PJ Keeling y TG Simdyanov (2002) La filogenia de los colpodélidos (Alveolata) que utilizan secuencias de genes de ARNr de subunidades pequeñas sugieren que son el grupo hermano de vida libre de los apicomplejos. Revista de Microbiología Eucariota 49: 498-504 .Wilson, RJM (2002) Progreso con plastidios parásitos. Revista de Biología Molecular 319: 257-274 .Moore, RB, M. Obornik, J. Janouskovec, T. Chrudimsky, M. Vancova, DH Green, SW Wright, NW Davies, CJS Bolch, K. Heimann, J. Slapeta, O. Hoegh-Guldberg, JM Logsdon y DA Carretero (2008). Un alveolado fotosintético estrechamente relacionado con los parásitos apicomplejos. Naturaleza 451: 959-963 . La otra conexión entre las algas y los apicomplejos es un remanente de cloroplasto, llamado apicoplasto, que se encuentra en la mayoría de los apicomplejos (2). El apicoplasto es probablemente el resultado de una endosimbiosis secundaria de un alga roja y probablemente sea el mismo evento endosimbiótico que da lugar a los plastidios de los dinoflagelados. El apicoplasto no es fotosintético, pero exhibe actividades asociadas con la biosíntesis de ácidos grasos tipo II, la biosíntesis de isoprenoides y posiblemente la síntesis de hemo. Estas vías son esencialmente procarióticas y representan excelentes objetivos farmacológicos. También se ha identificado un alveolado fotosintético, Chromera velia , que parece ser el apicomplejo de ramificación más temprana (3).Kuvardina, ON, BS Leander, VV Aleshin, AP Myl’nikov, PJ Keeling y TG Simdyanov (2002) La filogenia de los colpodélidos (Alveolata) que utilizan secuencias de genes de ARNr de subunidades pequeñas sugieren que son el grupo hermano de vida libre de los apicomplejos. Revista de Microbiología Eucariota 49: 498-504 .Wilson, RJM (2002) Progreso con plastidios parásitos. Revista de Biología Molecular 319: 257-274 .Moore, RB, M. Obornik, J. Janouskovec, T. Chrudimsky, M. Vancova, DH Green, SW Wright, NW Davies, CJS Bolch, K. Heimann, J. Slapeta, O. Hoegh-Guldberg, JM Logsdon y DA Carretero (2008). Un alveolado fotosintético estrechamente relacionado con los parásitos apicomplejos. Naturaleza 451: 959-963 . |
COCCIDIA
Los coccidios se caracterizan por una etapa de ooquiste de paredes gruesas que normalmente se excreta con las heces. Algunos coccidios ( Cryptosporidium, Cyclospora, Isospora ) realizan todo su ciclo de vida dentro de las células epiteliales intestinales del huésped y se transmiten por vía fecal-oral. Otros coccidios ( Sarcocystis, Toxoplasma ) tienen un ciclo de vida más complicado que involucra quistes tisulares y múltiples huéspedes (es decir, heteroxenos).
Criptosporidio
Desde su identificación inicial en 1907, se han identificado varias especies de Cryptosporidium en una amplia variedad de animales, desde peces hasta humanos. Los primeros casos humanos de criptosporidiosis se informaron en 1976 y se caracterizaron como una enfermedad diarreica asociada con supresión inmune. Inicialmente se creía que se trataba de una enfermedad rara y exótica. Durante la década de 1980, el Cryptosporidium fue reconocido como una de las principales causas de diarrea en pacientes con SIDA y, a menudo, provocaba la muerte. Sin embargo, ahora se reconoce que Cryptosporidium es una causa común de diarrea en personas inmunocompetentes y probablemente ha sido un patógeno humano desde el comienzo de la humanidad. Se han identificado dos especies que infectan a los humanos: C. parvum y C. hominis .
CICLO VITAL
Cryptosporidium a menudo se clasifica como coccidio y exhibe un ciclo de vida similar al de otros coccidios intestinales. Sin embargo, Cryptosporidium está más estrechamente relacionado con las gregarinas y esto se refleja en algunos aspectos de su ciclo de vida. La infección se adquiere mediante la ingestión de ooquistes esporulados (Figura). [ Ver figura más grande del ciclo de vida con leyenda detallada .] Los cambios de pH asociados con el paso a través del intestino y los fluidos biliares y pancreáticos en el intestino delgado desencadenan la excistación. Los esporozoítos (Sz) emergen del ooquiste y se adhieren a las células epiteliales intestinales. A diferencia de otros coccidios, los esporozoitos de Cryptosporidium no invaden los enterocitos. En cambio, inducen la fusión y expansión de las microvellosidades, lo que hace que el parásito quede rodeado por una doble membrana de origen del huésped. Se forma una unión, llamada “orgánulo alimentador” o “zona de adhesión”, entre el parásito y el enterocito huésped. El parásito, ahora llamado trofozoíto (Tr), probablemente obtiene nutrientes de la célula huésped a través de esta unión. (Para una revisión del proceso de “invasión”, ver Borowski et al, 2008. )
Los trofozoitos experimentan una replicación asexual (es decir, merogonía) y producen de 4 a 8 merozoitos (Mz) que se liberan en la luz intestinal. Los merozoítos infectan nuevas células epiteliales intestinales y se someten a rondas adicionales de merogonía. La mayor gravedad de la enfermedad en pacientes inmunocomprometidos se debe en parte a su incapacidad para limitar estas rondas adicionales de merogonía.
Como alternativa a la merogonía, los merozoitos pueden convertirse en macro o microgametocitos tras la infección de un enterocito. La microgametogénesis implica varias rondas de replicación seguidas de la liberación de numerosos microgametos en la luz intestinal. Los microgametos fertilizan a los macrogametos que aún están adheridos a las células epiteliales intestinales. El cigoto resultante (Zg) sufre esporogonia y los oocistos esporulados (Oo) se excretan con las heces. También es posible una autoinfección y esto también puede contribuir a una mayor gravedad de la enfermedad en pacientes inmunocomprometidos.
TRANSMISIÓN Y EPIDEMIOLOGÍA MOLECULAR
Los factores de riesgo de transmisión de Cryptosporidium son similares a los de otras enfermedades fecal-orales. Sin embargo, los brotes de criptosporidiosis transmitida por el agua han sido especialmente notables. El más infame es un brote en Milwaukee durante la primavera de 1993 en el que se estima que 400.000 personas desarrollaron criptosporidiosis sintomática (MacKenzie et al, New Eng. J. Med. 331:161, 1994 ). Los factores que contribuyen al mayor riesgo de brotes de Cryptosporidium transmitidos por el agua son: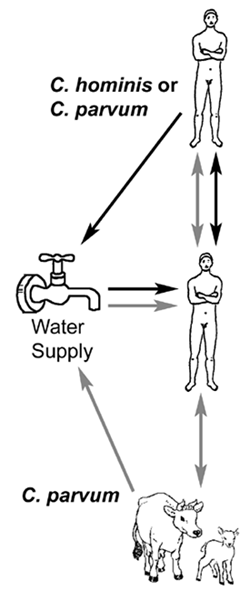
- tamaño pequeño de ooquistes
- Amplia gama de especificidad del huésped y desarrollo monoxeno.
- estrechas asociaciones entre huéspedes humanos y animales
- gran cantidad de ooquistes excretados (hasta 100 mil millones por ternero)
- dosis infecciosa baja
- Ooquistes robustos y resistentes al cloro.
- oocistos esporulados infecciosos excretados
A pesar de lo impresionantes de algunos brotes transmitidos por el agua, la transmisión de persona a persona parece predominar. Por ejemplo, los niños infectados asintomáticos son comunes, los casos secundarios en los hogares son elevados y los brotes tienden a ocurrir en hospitales, instituciones y guarderías, situaciones típicas de la transmisión fecal-oral . Los estudios moleculares han revelado dos genotipos primarios aislados de humanos. El genotipo 1 sólo se ha aislado de fuentes humanas y no es infeccioso para ratones y terneros. El genotipo 2 se ha aislado tanto de fuentes animales (bovinas y ovinas) como humanas y es infeccioso para ratones y terneros. Basándose en estas y otras diferencias biológicas, se ha propuesto cambiar el nombre del genotipo 1 a Cryptosporidium hominis (Morgan-Ryan et al, J. Euk. Microbiol. 49:433, 2002 ). Se han aislado otras especies y genotipos de Cryptosporidium (p. ej., C. felis , genotipo parecido a un perro, etc.) de pacientes con SIDA y, con poca frecuencia, de humanos inmunocompetentes (Morgan et al, J. Clin. Microbiol. 38:1180, 2000). También se ha propuesto una tercera especie del subcontinente indio, C. viatorum (Elwin et al, Int. J. Parasitol. 42:675, 2012 ).
Los datos genéticos implican que hay dos ciclos de transmisión distintos en humanos que involucran dos poblaciones diferentes de Cryptosporidium : 1) un ciclo exclusivamente antroponótico (es decir, de humano a humano) causado por el genotipo 1 (o C. hominis ) y 2) un ciclo zoonótico causada por el genotipo 2 (o C. parvum ). El ciclo zoonótico implicaría inicialmente la transmisión de animales (por ejemplo, vacas u ovejas) a humanos y luego, posteriormente, transmisión de persona a persona y posiblemente una transmisión de persona a animal. Se ha demostrado que ambos genotipos son el agente etiológico de los brotes transmitidos por el agua. Los brotes transmitidos por el agua relacionados con C. hominis probablemente se deban a la contaminación del agua con aguas residuales humanas, mientras que los brotes transmitidos por el agua asociados con C. parvum (genotipo 2) probablemente se deban a la contaminación del agua con heces de vaca u oveja.
PATOGÉNESIS
La manifestación clínica más común de la criptosporidiosis es una diarrea acuosa de leve a profusa. Esta diarrea generalmente desaparece espontáneamente y persiste desde varios días hasta un mes. Los recrudescencias son comunes. Calambres abdominales, anorexia, náuseas, pérdida de peso y vómitos son manifestaciones adicionales que pueden ocurrir durante la etapa aguda. La enfermedad puede ser mucho más grave para las personas con SIDA y se manifiesta como una diarrea crónica que dura meses o incluso años. Algunos pacientes de SIDA presentan una enfermedad fulminante parecida al cólera que requiere terapia de rehidratación intravenosa. La tasa de letalidad puede ser bastante alta en estos casos fulminantes.
La diarrea puede tener componentes osmóticos, inflamatorios o secretores (ver recuadro). La naturaleza acuosa de la diarrea asociada con las infecciones por Cryptosporidium ha sugerido la presencia de una enterotoxina. Sin embargo, no hay evidencia de diarrea secretora mediada por toxinas a pesar de los esfuerzos por identificar dicha toxina. La evidencia experimental sugiere que la absorción de Na + acoplada a glucosa disminuye y la secreción de Cl- aumenta . Por lo tanto, la diarrea asociada con Cryptosporidium parece ser principalmente de naturaleza osmótica (ver Figura). Asociado con esta alteración de la función de los enterocitos (es decir, las células epiteliales intestinales), hay un embotamiento de las vellosidades y una hiperplasia de las células de las criptas. Un posible mecanismo de patogénesis es que la infección de las células epiteliales intestinales con Cryptosporidium daña los enterocitos y eventualmente conduce a su muerte. Esto desencadena la división celular en la región de las criptas (es decir, hiperplasia) para reemplazar las células dañadas. La combinación de la destrucción de las células absorbentes en las puntas de las vellosidades y el aumento de la cripta secretora de Cl conduce a un aumento general de la secreción.
| Aspectos de la diarreaosmóticocaracterizado por mal funcionamiento de los enterocitos, por ejemplo:↓ Absorción de Na +→ Cl – secrecióninflamatoriogeneralmente asociado con invasión de la mucosainflamación de la lámina propialeucocitos en las hecessecretorgeneralmente asociado con enterotoxinas bacterianascaracterizado por diarrea acuosa | 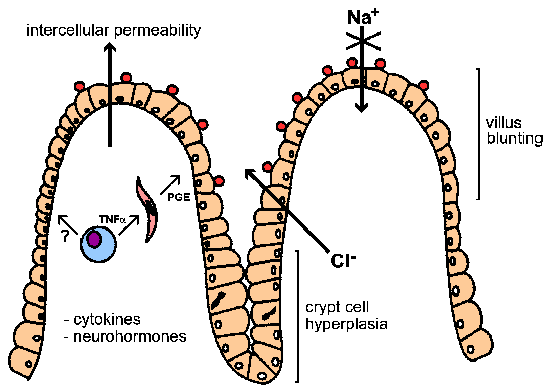 Representación esquemática de la patogénesis de Cryptosporidium . Muchos factores pueden estar involucrados en la diarrea asociada con la criptosporidiosis. (Modificado de Clark y Sears, Parasitology Today 12:221, 1996.) Representación esquemática de la patogénesis de Cryptosporidium . Muchos factores pueden estar involucrados en la diarrea asociada con la criptosporidiosis. (Modificado de Clark y Sears, Parasitology Today 12:221, 1996.) |
Además, un aumento de la permeabilidad intercelular y la inflamación en la capa submucosa (también conocida como lámina propia) se han asociado con la infección por Cryptosporidium . Este fenómeno también podría contribuir al proceso secretor a través de citoquinas y neurohormonas. Por ejemplo, los macrófagos que secretan factor de necrosis tumoral alfa (TNF-α) u otras citocinas pueden estimular a los fibroblastos y otras células de la lámina propia para que secreten prostoglandinas (PGE) y otros productos (p. ej., intermediarios reactivos del oxígeno). Estos productos pueden entonces promover la secreción y perjudicar la absorción.
El parásito muestra un trofismo por el yeyuno y el íleon en personas inmunocompetentes, mientras que la infección está más extendida en pacientes con SIDA y puede incluir el estómago, el duodeno, el colon y las vías biliares. Esta gama anatómica más amplia en los pacientes con SIDA se debe presumiblemente a la incapacidad del sistema inmunológico para controlar y limitar la infección. La inmunidad mediada por células parece ser el componente principal de la respuesta inmune para eliminar la infección, como lo demuestra la correlación entre un nivel más bajo de células T CD4+ y el riesgo y la gravedad de la criptosporidiosis. El interferón gamma, la interleucina-12 y el factor de necrosis tumoral alfa participan en la protección contra la infección por Cryptosporidium .
REFERENCIAS ADICIONALES
- Clark DP, Sears CL (1996) La patogénesis de la criptosporidiosis. Parasitología Hoy 12:221
- Guerrant RL (1997) Criptosporidiosis: una amenaza emergente y altamente infecciosa. Emergente. inf. Dis. 3:51
- Greg Hannahs, Cryptosporidium parvum : un patógeno emergente. http://biology.kenyon.edu/slonc/bio38/hannahs/crypto.htm
- NE Ramirez, LA Ward y S Sreevatsan (2004) Una revisión de la biología y epidemiología de la criptosporidiosis en humanos y animales. Microbios e infecciones 6, 773-785 .
- Rose JB, Huffman DE, Gennaccaro A (2002) Riesgo y control de la criptosporidiosis transmitida por el agua. Microbiol FEMS. Apocalipsis 26:113 .
- Sunnotel, O et al (2006) Cryptosporidium . Cartas de Microbiología Aplicada 43, 7-16 .
- Xiao L y Ryan UM (2004) Criptosporidiosis: una actualización en epidemiología molecular. Opiniones actuales sobre enfermedades infecciosas 17, 483-490 .
- Xiao, L. y Feng, Y. (2008) Criptosporidiosis zoonótica. FEMS Inmunología y microbiología médica 52: 309-323 .
Isóspora
Se cree que Isospora belli es una especie válida que sólo infecta a los humanos. Tiene una distribución mundial pero es más común en regiones tropicales y áreas con saneamiento deficiente. Las infecciones suelen ser asintomáticas y las que presentan síntomas tienden a desaparecer espontáneamente con una duración de unas pocas semanas. Las infecciones son más comunes y los síntomas más graves en los pacientes con SIDA que en las personas inmunocompetentes.
Ciclo vital . La infección se adquiere mediante la ingestión de ooquistes esporulados (sOo). Los esporozoitos (Sz) se liberan en la luz intestinal e invaden las células epiteliales intestinales. Dentro de las células epiteliales, el parásito sufre una ronda de merogonía que conduce a la producción de merozoítos (Mz). Los merozoítos liberados vuelven a invadir las células epiteliales intestinales y pueden sufrir rondas adicionales de merogonía o convertirse en micro o macrogamontes. Los microgametos (ga) fertilizarán a los macrogametos (ga) para formar un cigoto (Zy) que se desarrollará hasta convertirse en el ooquiste (Oo). Los ooquistes inmaduros se eliminan con las heces y la maduración hasta convertirse en ooquistes esporulados infecciosos se produce en el medio ambiente. Las etapas reconocibles durante esta maduración (es decir, esporogonia) incluyen ooquistes con un solo esporoblasto, ooquistes con dos esporoblastos y el ooquiste maduro con dos esporoquistes, cada uno de los cuales contiene cuatro esporozoitos. [Ver también una discusión detallada sobre el ciclo de vida de Cryptosporidium ].
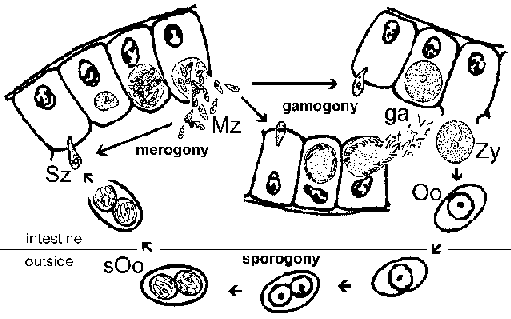
Síntomas y patogenia . Los síntomas asociados con la infección por I. belli incluyen diarrea, esteatorrea, dolor de cabeza, fiebre, dolor abdominal, náuseas, deshidratación y pérdida de peso. Rara vez hay sangre en las heces. En general, los síntomas son similares a los de la criptosporidiosis. La enfermedad suele ser autolimitada. Sin embargo, puede volverse crónico, detectándose ooquistes en las heces durante meses o años y recrudecimiento de los síntomas. La enfermedad tiende a ser más grave en bebés y niños pequeños que en adultos. La patología asociada con las infecciones por I. belli es principalmente atrofia o embotamiento de las vellosidades e hiperplasia de las criptas, como se observa comúnmente en otras infecciones intestinales.
La diarrea de los pacientes con SIDA suele ser muy acuosa y puede provocar deshidratación que requiere hospitalización. La fiebre y la pérdida de peso también son un hallazgo común. Otro hallazgo común entre los pacientes con SIDA es una diarrea crónica intermitente que dura meses o años. La pérdida excesiva de peso resultante y el desequilibrio electrolítico pueden provocar emaciación e incluso la muerte. También ha habido algunos informes de isosporiasis extraintestinal diseminada en pacientes con SIDA.
Lindsay, DS, Dubey, JP, Blagburn, BL (1997) Biología de Isospora spp. de humanos, primates no humanos y animales domésticos. Clínico. Microbiol. Apocalipsis 10: 19-34 .
Ciclospora
Los primeros casos humanos de Cyclospora cayetanensis se informaron en 1979. Originalmente se la conocía como cuerpos similares a cianobacterias o cuerpos similares a coccidios (CLB). Se confirmó que el organismo era un parásito coccidio con una estructura de oocistos similar al género Cyclospora y luego recibió el nombre en 1994 de la Universidad Peruana Cayetano Heredia en Perú, donde se habían llevado a cabo la mayoría de los primeros estudios. Los estudios moleculares indican una estrecha relación con Eimeria, un importante parásito veterinario de las aves de corral y otros animales. C. cayetanenis tiene una distribución mundial, pero parece ser especialmente frecuente en América Latina, el subcontinente indio y el sudeste asiático. En los países desarrollados, las infecciones suelen estar asociadas con brotes transmitidos por alimentos o con diarrea del viajero.
Ciclo de vida y transmisión . El ciclo de vida de Cylcospora es similar al de Isospora ( ver arriba ). La infección se adquiere mediante la ingestión de ooquistes. Los esprorozoítos se liberan e infectan las células epiteliales de la parte superior del intestino delgado. El parásito sufre merogonía y los merozoitos reinfectan los enterocitos y pueden ocurrir varias rondas más de merogonía. Algunos de los merozoítos experimentan un desarrollo sexual que da como resultado la producción de micro y macrogametos. La fertilización del macrogameto por el microgameto inicia la esporogonia y la formación del ooquiste. Al igual que Isospora , la esporulación se completa en el ambiente y los oocistos inmaduros no infecciosos se excretan en las heces. La maduración de los ooquistes a ooquistes infecciosos esporulados probablemente lleva días o semanas. Además, la estructura del ooquiste de Cyclospora es diferente a la de Isospora . El ooquiste contiene dos esporoquistes, cada uno de los cuales contiene dos esporozoitos.
Varios brotes en Estados Unidos y Canadá se han asociado con productos frescos importados de América del Sur y Central (Tabla). En particular, se han identificado bayas y verduras de hoja como elementos probablemente contaminados. Estos son alimentos que normalmente se comen crudos y sólo se enjuagan. No se han asociado brotes con frutas o verduras congeladas, procesadas o peladas. También se ha observado una estacionalidad en los brotes y la mayoría de los casos ocurren en la primavera y principios del verano. También se ha observado una estacionalidad similar en los países endémicos. A diferencia de Estados Unidos y Canadá, donde predomina la transmisión alimentaria, la mayoría de los casos en Europa y Australia se han asociado con viajes a países endémicos.
| Brotes seleccionados de ciclosporiasis en Estados Unidos y Canadá |
| FechaUbicaciónVehículoFuentemayo-95Floridaframbuesa¿Guatemala?Mayo JunioEstados Unidos, puedeframbuesasGuatemalamarzo-abrilFloridamezclum¿Perú?Abril MayoEstados Unidos, CanadáframbuesasGuatemalaJunio Juliolavadoalbahacadesconocidoseptiembre-97Virginiaplato de frutasdesconocidoDic-97FloridamezclumPerúmayo-98ontarioframbuesasGuatemalamayo-98Georgia¿ensalada de frutas?desconocidomayo-99ontariopostre de bayadesconocidomayo-99Floridafruta (baya)desconocidojulio-99MisurialbahacaMéxico o Estados Unidosjunio-00PensilvaniaframbuesasGuatemalamayo-01coronel británicoalbahacaTailandiaMayo JunioPensilvaniaguisantesGuatemalaModificado de Herwaldt (2000) y actualizado. Los signos de interrogación (?) indican vehículo o fuente probable, pero no confirmado. |
Como resultado del elevado número de brotes asociados con las frambuesas de Guatemala, Estados Unidos restringió la importación de frambuesas y exigió inspección de las granjas. Esto resultó en una caída posterior en el número de brotes en los Estados Unidos. Canadá, que no restringió las importaciones, no experimentó una disminución en el número de brotes durante este período. Estudios posteriores de casos controlados realizados en Guatemala revelaron que las infecciones eran más comunes en los niños y la prevalencia alcanzó su punto máximo en junio. El principal factor de riesgo asociado con la infección fue beber agua sin tratar. En Perú se identificó el contacto con el suelo como otro factor de riesgo, especialmente entre niños menores de dos años. Un tratamiento inadecuado del agua en estos países endémicos puede provocar la contaminación de las aguas subterráneas y, por tanto, mantener el ciclo de transmisión. Presumiblemente, la transmisión a través de los alimentos se debe al riego o la aplicación de fertilizantes con agua contaminada o al lavado y procesamiento de alimentos con agua mal tratada.
Síntomas . Cyclospora infecta principalmente las células epiteliales de la porción superior del intestino delgado. El período de incubación es generalmente de una a dos semanas. Los síntomas son similares a los de la gastroenteritis causada por Isospora y Cryptosporidium , que normalmente incluye ciclos de diarrea acuosa y períodos de aparente remisión. La diarrea se caracteriza por deposiciones frecuentes y puede persistir hasta seis semanas, pero generalmente desaparece espontáneamente en personas inmunocompetentes. Anorexia, malestar general, náuseas y calambres son otros síntomas frecuentes asociados a la ciclosporiasis. En algunos casos, los pacientes pueden experimentar vómitos, dolores musculares, pérdida sustancial de peso y diarrea explosiva. La exposición previa a Cyclospora parece conferir cierta resistencia a la infección con una disminución de los síntomas. Con el tiempo, los adultos parecen desarrollar inmunidad y se pueden encontrar portadores asintomáticos en áreas endémicas.
Al igual que Cryptosporidium e Isospora , la diarrea provocada por Cyclospora en pacientes con SIDA es mucho más grave que en personas inmunocompetentes. La diarrea puede durar meses y producir un síndrome debilitante y potencialmente mortal.
Reseñas de ciclospora:
Sterling y Ortega (1999) Clycospora : un enigma que vale la pena desentrañar. Emergente. inf. Dis. 5:48 .
BL Herwaldt (2000) Cyclospora cayetanensis : una revisión centrada en los brotes de ciclosporiasis en la década de 1990. Clínico. inf. Dis. 31:1040 .
JM Shields y BH Olson (2003) Cyclospora cayetanensis: una revisión de un coccidio parásito emergente. Revista Internacional de Parasitología 33, 371-391 .
LS Mansfield y AA Gajadhar (2004) Cyclospora cayetanensis , un parásito coccidio transmitido por los alimentos y el agua. Parasitología Veterinaria 126: 73-90 .
YR Ortega y R Sanchez (2010) Cyclospora cayetanensis , un parásito transmitido por los alimentos y el agua. Clínico. Microbiol. Apocalipsis 23:218-234 .
Diagnóstico y tratamiento de coccidias intestinales
La coccidiosis se diagnostica al demostrar ooquistes en las heces. La tinción acidorresistente es el método preferido para los coccidios que se tiñen de rojo brillante. Cryptosporidium, Cyclospora e Isospora se distinguen por el tamaño y la estructura de los oocistos (Tabla). Cyclospora e Isospora no absorben uniformemente el tinte, lo que da como resultado una mezcla de ooquistes sin teñir, parcialmente teñidos y completamente teñidos. Cyclospora e Isospora también se pueden detectar mediante una autofluorescencia asociada con la pared del quiste. Debido a su tamaño relativamente grande, Isospora se detecta fácilmente en muestras no teñidas. Sarcocystis es una infección humana poco común ( ver más abajo ) con ooquistes similares a Isospora , excepto que los esporoquistes generalmente se liberan de los ooquistes mientras aún se encuentran en la luz intestinal.
| Parásitos coccidios encontrados en las heces humanas |
|---|
| EspeciesForma excretadaTamaño (μm)Estructura del ooquistecriptosporidioooquistes esporulados4-54 esporozoitos, sin esporoquistesciclosporaooquistes no esporulados8-102 esporoquistes con 2 esporozoítos cada unoisósporaooquistes no esporulados30 x 122 esporoquistes con 4 esporozoítos cada unoSarcocistisesporocistos esporulados13 x 102 esporoquistes con 4 esporozoítos cada uno |
El tratamiento recomendado para Cyclospora e Isospora es la combinación de trimetoprim-sulfametoxazol (Bactrim). No existe un tratamiento completamente satisfactorio para Cryptosporidium . Se plantea la hipótesis de que la ubicación “extracitoplasmática” de Cryptosporidium lo protege de las drogas. La paromomicina se ha utilizado para el tratamiento de la criptosporidiosis; sin embargo, se debate su eficacia. Los estudios controlados indican que la paromomicina suprime modestamente la parasitemia en individuos inmunocomprometidos. El tratamiento de la criptosporidiosis grave debe incluir cuidados de apoyo (rehidratación y apoyo nutricional) y agentes antimotilidad. Las medidas preventivas serán similares a otras enfermedades transmitidas por vía fecal-oral (ver factores de riesgo o control de Giardia ).
Quistes tisulares que forman coccidias
Algunas especies de coccidios exhiben un ciclo de vida heteroxeno en el que la merogonía tiene lugar en los tejidos del huésped intermedio (presa) y la gametogonía tiene lugar en el epitelio intestinal del huésped definitivo (depredador). [Por convención, la reproducción sexual ocurre en huéspedes definitivos.] En lo que respecta a las infecciones humanas, Toxoplasma es un quiste tisular común que forma un parásito coccidio, mientras que las infecciones con especies de Sarcocystis son bastante raras.
El ciclo de vida (ver Figura) de Sarcocystis dentro del depredador (es decir, carnívoro) es similar a los ciclos de vida de los coccidios intestinales, como Isospora , e implica un ciclo sexual (gametogonía) dentro de las células epiteliales intestinales. Una diferencia en el ciclo de vida de Sarcocystis es la falta de merogonia en las células epiteliales intestinales. En otras palabras, los merozoítos adquiridos al ingerir una presa infectada sólo producirán gametos tras la invasión de las células epiteliales intestinales. La fusión de los gametos conduce a la producción de ooquistes. Además, los esporoquistes suelen liberarse de los ooquistes dentro del intestino del huésped y, por tanto, se encuentran esporoquistes infecciosos en las heces.
Los huéspedes intermediarios (herbívoros) adquieren la infección al ingerir los esporocistos esporulados. Los esporozoítos se liberan, invaden las células epiteliales intestinales y sufren merogonía como es típico de los coccidios intestinales. A diferencia de los coccidios intestinales, los merozoitos invadirán las células endoteliales y producirán una infección sistémica. Muy a menudo existe un tropismo por tejidos particulares como el cerebro o los músculos. Los merontos (o esquizontes) de estos tejidos suelen estar encapsulados y se denominan “quistes tisulares”. Estos quistes tisulares, o sarcoquistes en el caso del músculo, a menudo exhiben un nivel más bajo de replicación durante la merogonía y están algo inactivos. La ingestión del animal infectado por un carnívoro liberará los merozoitos que invadirán las células epiteliales intestinales y completarán así el ciclo de vida.

Este ciclo de vida depredador-presa no se resolvió hasta los años 1970. Anteriormente, las infecciones intestinales en el depredador generalmente se designaban como especies de Isospora y las infecciones tisulares en las presas generalmente se designaban como especies de Sarcocystis . En muchos casos, los huéspedes definitivos no han sido identificados positivamente y la taxonomía de muchas especies de Sarcocystis es incierta.
Se han documentado infecciones por Sarcocystis en humanos, pero son poco comunes. Los seres humanos son el huésped definitivo de S. hominis (también conocido como S. bovihominis ) y S. suihominis , según lo determinado por el hecho de que la fuente de infección sea carne de res o cerdo, respectivamente. La ingestión de carne de vacuno o de cerdo poco cocida procedente de animales infectados producirá una infección entérica que puede producir síntomas intestinales agudos (malestar abdominal, náuseas, diarrea). Sin embargo, se cree que la mayoría de las infecciones son asintomáticas. Las personas infectadas pueden eliminar esporocistos en las heces durante semanas o meses después de la infección. Los esporocistos de las heces humanas son infecciosos para las vacas, los cerdos y los ciervos.
Los humanos también pueden servir como huéspedes intermediarios de al menos algunas de las especies de Sarcocystis que se encuentran en la naturaleza. La ingestión de esporoquistes por parte de humanos puede provocar la fase tisular de la infección y la formación de sarcoquistes. Estos sarcoquistes suelen tener un tamaño de varias 100 µm y causan poco daño tisular. Los síntomas clínicos pueden incluir sensibilidad muscular o hinchazones inflamatorias dolorosas episódicas. Estos quistes musculares en humanos sólo se han notificado esporádicamente (<100 casos notificados) y probablemente representan infecciones accidentales. Un estudio observó que los sarcoquistes en humanos tendían a parecerse a las especies de Sarcocystis que se encuentran comúnmente en monos locales (Beaver et al, Am. J. Trop. Med. Hyg. 28:819, 1979). La mayoría de los casos se han notificado en Asia tropical y subtropical, incluido un brote de sarcocistosis muscular entre viajeros que regresaban de Malasia ( MMWR 61:37 ).
Fayer, R (2004) Sarcocystis spp. en Infecciones Humanas. Clínico. Microbiol. Apocalipsis 17: 894-902 .
TOXOPLASMOSIS
Toxoplasma gondii es un parásito coccidio que infecta a los humanos y a una amplia variedad de mamíferos y aves. Exhibe un ciclo de vida de tipo depredador-presa (como se analizó anteriormente para Sarcocystis ) y los felinos son el único huésped definitivo. La toxoplasmosis se encuentra en todo el mundo (excepto en climas extremadamente fríos o secos) y tiende a ser más frecuente en climas tropicales. Los estudios serológicos han demostrado tasas de prevalencia de hasta el 70% a la edad de 25 años en algunas poblaciones centroamericanas. En los Estados Unidos, se estima que entre el 0,5% y el 1% de la población se infecta cada año y la prevalencia oscila entre el 10% y el 25% a la edad de 25 años. La toxoplasmosis suele ser una enfermedad benigna. Se observan excepciones en los casos de infección congénita o de personas inmunocomprometidas .
- Ciclo vital
- Transmisión humana
- Expansión reciente de Toxoplasma
- Características clínicas
- Congénito
- Ocular
- Diagnóstico , Tratamiento y Prevención
Ciclo vital
Toxoplasma tiene un ciclo de vida complejo que consta de fases intestinales y tisulares. Aunque el organismo se descubrió por primera vez en 1908 como un parásito tisular del gondi (un roedor africano), su ciclo de vida completo no se determinó hasta 1970. La fase intestinal de la infección ocurre sólo en felinos y exhibe un ciclo de vida coccidio intestinal típico que consiste en de merogonía y gamogonía (ver ciclo de vida de Isospora ). Los gatos adquieren la infección al comer animales infectados con la fase tisular del parásito. Los parásitos invaden las células epiteliales intestinales y sufren merogonía. Los merozoitos resultantes pueden someterse a rondas adicionales de merogonía o gametogonía. Como es similar a otros apicomplejos (ver ciclo de vida general de los apicomplejos ), se producen macro y microgametos. Así, el gato es considerado el huésped definitivo ya que es éste el huésped en el que se produce el ciclo sexual.
Los microgametos biflagelados se liberan en la luz del intestino y fertilizan los macrogametos dentro de las células epiteliales del huésped. La secreción de la pared del ooquiste comienza poco después de la fertilización. Este ciclo sexual culmina con la producción de ooquistes que se excretan en las heces. Estos ooquistes inmaduros sufren esporogonia a temperatura ambiente, lo que da como resultado ooquistes maduros que contienen dos esporoquistes, cada uno con cuatro esporozoitos. La esporulación generalmente demora de 1 a 4 días y los ooquistes permanecen infecciosos durante meses en suelo húmedo y sombreado. Se ha planteado la hipótesis de que los macrogametos no fertilizados también pueden ser capaces de formar oocistos maduros ( Ferguson, Tr. Parasitol. 18:351, 2002 ).
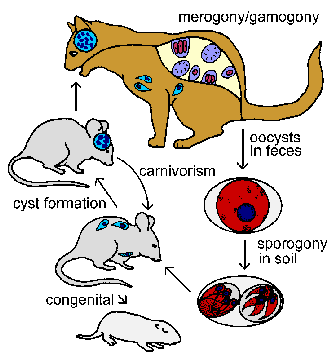
Los huéspedes intermediarios, como roedores y aves, se infectan mediante la ingestión de ooquistes esporulados. Los esporozoitos se liberan, penetran en el epitelio intestinal e invaden los macrófagos y otros tipos de células. El proceso de invasión es típico de apicomplexa y el parásito se encuentra dentro de una vacuola parasitófora. Dentro de la vacuola, el parásito sufre una fisión binaria (es decir, merogonía) mediante un proceso único llamado endodiogenia. La endodiogenia es un tipo especializado de división en el que las dos células hijas se forman dentro de la célula madre. Estas formas tróficas se denominan taquizoítos ( taqui significa rápido) en referencia a su alto nivel de replicación. La célula huésped se romperá y liberará los taquizoitos que invadirán nuevas células huésped y repetirán el ciclo replicativo. Los macrófagos infectados diseminarán los taquizoítos por todo el huésped durante esta infección aguda.
A medida que el huésped desarrolla inmunidad, la tasa de replicación se ralentizará y las células infectadas del huésped quedarán encapsuladas (es decir, quistes tisulares). Estas formas que se replican lentamente se denominan bradizoítos ( brady significa lento) y representan una etapa latente o de reposo. Se considera que los bradizoítos están metabólicamente inactivos, pero siguen siendo viables ( Dubey et al, Clin. Microbiol. Rev. 11:267, 1998 ). Otros cambios que ocurren cuando los taquizoítos se convierten en bradizoítos incluyen la secreción de quitina y otros componentes para formar la pared del quiste y la acumulación de gránulos de amilopectina (que reflejan el almacenamiento de glucosa). Los quistes tisulares de Toxoplasma exhiben una variedad de tamaños, pero a menudo alcanzan un tamaño de 50 a 70 µm de diámetro y contienen entre 1000 y 2000 bradizoítos. Los bradizoítos se encuentran principalmente en el cerebro y el tejido muscular, mientras que los taquizoítos tienden a encontrarse en las células reticuloendoteliales.La etapa de bradizoíto representa una infección crónica y probablemente persiste durante toda la vida del huésped. Se desconoce el mecanismo de esta persistencia. Algunos investigadores creen que los quistes tisulares se descomponen periódicamente y liberan bradizoitos que invadirán nuevas células huésped y conducirán a la formación de más quistes tisulares.
La fase tisular de la infección también puede transmitirse de forma congénita a la descendencia y a otros huéspedes intermediarios mediante el carnivorismo. La ingestión de un animal infectado liberará los bradizoitos de los quistes tisulares que luego infectarán las células del nuevo huésped. Posiblemente todos los mamíferos, incluido el ser humano, puedan infectarse con Toxoplasma . Como en el caso de adquirir la infección por ingestión de ooquistes, los parásitos pasarán por una fase aguda caracterizada por una rápida replicación seguida de una fase crónica caracterizada por quistes tisulares latentes. La ingestión de un huésped intermediario infectado por parte del gato iniciará la etapa intestinal del ciclo de vida que involucra merogonía y gamogonía en las células epiteliales intestinales. Los gatos también pueden apoyar la etapa tisular de la infección.
| Transmisión humana |
|---|
| ingerir oocistosingerir etapas de tejidoleche cruda de cabracongénitotrasplante de organotransfusión de sangre |
Obviamente los humanos no somos una parte natural del ciclo de vida depredador-presa y representan un huésped accidental que no participa en la continuación del ciclo de transmisión. Una fuente de infección es la ingestión de material contaminado con oocistos esporulados excretados por los gatos. Esto implica cierta asociación con los gatos. Sin embargo, dado que los ooquistes necesitan madurar en el medio ambiente antes de volverse infecciosos, la transmisión incluirá características de transmisión en el suelo similares a las de Isospora y Cyclospora . Por ejemplo, se cree que los niños en edades que gatean y comen tierra corren un mayor riesgo de infección. Los ooquistes también se pueden adquirir a través de actividades de jardinería o de frutas o verduras sin lavar. Además, se han documentado algunos brotes transmitidos por el agua. Se cree que la alta prevalencia de toxoplasmosis en América del Sur y Central se debe a los altos niveles de contaminación del medio ambiente con ooquistes. Irónicamente, el contacto con perros es más un factor de riesgo para infectarse con Toxoplasma que el contacto con gatos. Es probable que esto se deba a que los perros buscan heces de gato y se contaminan con ellas y luego transfieren los ooquistes esporulados a la ropa y las manos de sus dueños. Curiosamente, se informó de un brote transmitido por el agua asociado con gatitos que vivían encima de un depósito de agua municipal en Brasil (de Moura et al, 2006, Emerg. Inf. Dis. 12:326 ).
La toxoplasmosis también se puede adquirir mediante la ingestión de carne poco cocida que contiene quistes tisulares o taquizoítos. Presumiblemente el ganado adquiere la infección al pastar en áreas contaminadas con heces de gato. La capacidad del parásito para transferirse entre huéspedes intermediarios puede ser una adaptación evolutiva relativamente reciente del parásito que coincide con la domesticación del gato y la expansión de la agricultura ( ver Cuadro ). De hecho, la mayoría de las infecciones entre adultos en Estados Unidos y Europa probablemente se adquieren por carne poco cocida. La tasa especialmente alta de seropositivos en Francia (hasta el 90%) probablemente se deba a una predilección cultural por la carne cruda o poco cocida. El cordero y el cerdo son fuentes más comunes que la carne de res. También ha habido algunos informes aislados de transmisión de Toxoplasma a través de taquizoítos en la leche de cabra no pasteurizada.
El toxoplasma también puede transmitirse de la madre al feto, a menudo con consecuencias nefastas ( ver más abajo ). La transmisión congénita sólo puede ocurrir durante una infección aguda (es decir, taquizoítos) adquirida durante el embarazo. Las madres con una infección crónica adquirida antes del embarazo no corren riesgo de transmitir Toxoplasma . También es posible la transmisión de Toxoplasma como resultado de trasplantes de órganos. Los quistes de tejido de un donante de órganos con infección crónica pueden reactivarse cuando se trasplantan a un receptor de órganos previamente no infectado. Además, la terapia inmunosupresora también podría reactivar una infección latente en el receptor. También es posible la adquisición de taquizoitos de una persona con infección aguda mediante transfusión de sangre. Sin embargo, la transmisión por trasplante o transfusión ahora es poco común.
| ¿ Expansión reciente de Toxoplasma ? |
|---|
| El análisis molecular de aislamientos de Toxoplasma (principalmente de América del Norte y Europa) revela una diversidad genética limitada. La mayoría (>94%) de los aislados se agrupan en tres linajes clonales distintos designados como Tipo I, Tipo II y Tipo III. Estos tres linajes clonales están estrechamente relacionados y se componen de varias mezclas de sólo dos alelos en los loci probados. Los tres tipos pueden haber surgido de una recombinación genética ocurrida en los últimos 10.000 años (1). Esto coincidiría con la expansión de la agricultura humana y la adaptación del gato doméstico. Así, los cambios en el comportamiento humano pueden haber conducido a una selección y rápida propagación de Toxoplasma . Además, todos estos tipos clonales exhiben la capacidad de transmitirse a través de una ruta oral directa entre huéspedes intermediarios, lo que puede no haber sido una característica biológica del Toxoplasma ancestral u otras especies estrechamente relacionadas como Neospora ( ver cuadro a continuación ). Esta adquisición de infectividad oral directa combinada con la domesticación de animales podría promover una expansión rápida, y principalmente asexual, de Toxoplasma .Los tres genotipos de Toxoplasma también presentan diferencias en virulencia (2). Por ejemplo, los parásitos tipo I son muy virulentos en ratones. De manera similar, el tipo I se asocia desproporcionadamente con toxoplasmosis ocular atípica grave en individuos inmunocompetentes y con toxoplasmosis congénita grave. Sin embargo, afortunadamente, las infecciones de tipo II tienden a dominar, especialmente en los EE. UU. Sin embargo, hay cierta evidencia que sugiere que Toxoplasma exhibe más diversidad en América del Sur. Las mejoras en nuestro conocimiento sobre la biología de la población de Toxoplasma pueden ayudar a resolver estos problemas y conducir a un mejor control y tratamiento. Su et al (2003) Expansión reciente de Toxoplasma a través de una transmisión oral mejorada. Ciencia 299, 414 .Boothroyd y Grigg (2002) Biología poblacional de Toxoplasma gondii y su relevancia para la infección humana: ¿diferentes cepas causan diferentes enfermedades? actual. Opinión. Microbiol. 5, 438 . |
Características clínicas
La toxoplasmosis en adultos y niños después de la etapa neonatal suele ser benigna y asintomática. La adquisición de la infección a través de ooquistes o quistes tisulares da como resultado una infección aguda en la que los taquizoitos se diseminan por todo el cuerpo a través de los vasos linfáticos y hematógenos. Esta etapa aguda persistirá durante varias semanas a medida que se desarrolle la inmunidad. La producción de anticuerpos requiere de 1 a 2 semanas y la inmunidad celular ocurre de 2 a 4 semanas después de la infección. Tanto la inmunidad humoral como la celular son importantes, pero la respuesta celular parece crítica para la conversión de una infección aguda (es decir, taquizoítos) a crónica (es decir, bradizoítos). (Consulte el ciclo de vida para obtener una explicación de los taquizoítos y los bradizoítos). En particular, una fuerte respuesta Th1 caracterizada por la producción de citocinas proinflamatorias que incluyen interleucina-12, interferón gamma y factor de necrosis tumoral alfa se asocia con la infección por Toxoplasma .
Cuando se presentan síntomas, generalmente son leves y típicamente se describen como similares a los de una mononucleosis con escalofríos, fiebre, dolor de cabeza, mialgia, fatiga e inflamación de los ganglios linfáticos. Estos síntomas son autolimitados y se resuelven en semanas o meses. También se ha observado como síntoma de toxoplasmosis una linpadenopatía crónica sin fiebre que persiste o recurre durante hasta un año. Rara vez los individuos inmunocompetentes presentan síntomas graves y la infección aguda casi siempre progresa a la etapa crónica. Esta infección latente probablemente persiste durante toda la vida del paciente sin producir ninguna patología progresiva.
| Encefalitis toxoplásmica |
|---|
| Las lesiones pueden detectarse con tomografía computarizada o resonancia magnética.sin IgM, los cambios en los títulos de IgG son impredeciblesno se propaga a otros órganosdebido a reactivación de infección latente, no adquirida |
La toxoplasmosis se ha observado desde hace mucho tiempo como una infección oportunista en lo que respecta a la reactivación de infecciones latentes debido a la inmunosupresión asociada con los trasplantes de órganos y ciertos tratamientos contra el cáncer. Durante la década de 1980, la encefalitis toxoplásmica surgió como una complicación común asociada con el SIDA. Se estima que entre el 25% y el 50% de los pacientes con SIDA y toxoplasmosis crónica desarrollarán encefalitis. La reactivación de la infección suele ocurrir cuando las células CD4 caen por debajo de 100 células por microlitro. Los primeros síntomas de la encefalitis toxoplásmica pueden incluir dolor de cabeza, fiebre, letargo y alteración del estado mental con progresión a déficits neurológicos focales y convulsiones. La enfermedad casi siempre se debe a la reactivación de una infección latente (véase el recuadro) y tiende a permanecer confinada al SNC. En otras palabras, los quistes tisulares se rompen y los bradizoítos liberados se transforman en taquizoítos. (Ver ciclo de vida para una explicación de taquizoítos y bradizoítos). Las lesiones focales son causadas por la destrucción de las células huésped en las inmediaciones. Ocasionalmente pueden aparecer otras formas de la enfermedad reactivada, especialmente retinocoroiditis, neumonitis, miocarditis y miositis, junto con la inmunosupresión.
Carlos S. Subauste, Toxoplasmosis y SIDA .
| Resultados de infecciones congénitas |
|---|
| 5-10% muerte (aborto o nacimiento muerto) 8-10% daño cerebral u ocular severo 10-13% discapacidades visuales de moderadas a severas 58-72% Asintomático al nacer, desarrollando retinocoroiditis o síntomas neurológicos más tarde. |
Toxoplasmosis congénita
El toxoplasma también puede transmitirse de forma congénita (es decir, transplacentaria) si la madre adquiere la infección durante el embarazo. Las infecciones congénitas (es decir, transplacentarias) tienen más probabilidades de ser sintomáticas que las infecciones posnatales y pueden ser particularmente graves (ver Cuadro de resultados). Algunas de las características más destacadas son:
- la transmisión solo es posible durante la etapa aguda (es decir, la infección primaria debe ocurrir durante el embarazo)
- solo puede ocurrir una vez
- Un tercio de las madres que se seroconvierten durante el embarazo transmitirán la infección al feto.
- incidencia entre 1 por 1.000 y 1 por 10.000 nacidos vivos
- La gravedad varía según la edad del feto (más grave al comienzo del embarazo).
- La transmisión es más frecuente más adelante en el embarazo.
- La infección puede provocar: aborto espontáneo, parto prematuro o parto a término con o sin enfermedad progresiva.
- Las manifestaciones típicas de la enfermedad incluyen: retinocoroiditis, calcificación intracerebral, hidrocefalia, microcefalia, trastornos psicomotores, retraso mental, ceguera y otros defectos visuales.
Toxoplasmosis ocular
La retinocoroiditis, inflamación de la retina y la coroides (área vascular gruesa en la parte posterior del ojo), es otra manifestación clínica de la infección por Toxoplasma . La retinocoroiditis puede deberse a infecciones congénitas o a infecciones agudas o reactivadas adquiridas posnatalmente. Originalmente las manifestaciones oculares se asociaban más frecuentemente a infecciones congénitas o a una manifestación tardía por reactivación de una infección congénita. Sin embargo, la toxoplasmosis ocular se informa con una frecuencia cada vez mayor en asociación con infecciones agudas. Se ha sugerido que diferentes genotipos exhiben diferentes niveles de virulencia, especialmente en lo que respecta a la expresión de enfermedades oculares. En el caso de una infección congénita, la retinocoroiditis puede desarrollarse semanas o años después del nacimiento. Aproximadamente el veinte por ciento de las personas con infecciones congénitas presentarán retinocoroiditis al nacer y en la adolescencia el 82% presentará síntomas.
Las lesiones son de naturaleza focal y generalmente autolimitadas. Se cree que son el resultado de la rotura de un quiste en la retina en los casos reactivados o de taquizoítos en los casos agudos. Las células de la retina se parecen mucho a las del sistema nervioso central. También pueden presentarse lesiones granulomatosas en la coroides. Las lesiones suelen ser bilaterales en las infecciones congénitas y unilaterales si se adquieren posnatalmente. Los estudios en animales proporcionan evidencia de que la necrosis retiniana asociada con la lesión es atribuible a la proliferación de parásitos, mientras que las respuestas de hipersensibilidad a los antígenos toxoplásmicos son responsables de la inflamación acompañante. Los síntomas pueden incluir visión borrosa u otros defectos visuales. La visión puede mejorar con la resolución de la inflamación. Se han observado recurrencias de la enfermedad, pero la frecuencia y los factores que influyen en la recurrencia no están claros. La enfermedad rara vez es progresiva en personas inmunocompetentes, pero puede dejar cicatrices en la retina. Sin embargo, la enfermedad puede ser bastante grave en los pacientes con SIDA y seguir progresando.
- GN Holland (2003) Toxoplasmosis ocular: una reevaluación global: parte I: epidemiología y curso de la enfermedad. Revista Estadounidense de Oftalmología 136, 973-988 .
- GN Holland (2004) Toxoplasmosis ocular: una reevaluación global: parte II: manifestaciones y manejo de la enfermedad. Revista Estadounidense de Oftalmología 137, 1-17 .
Diagnóstico, Tratamiento y Prevención
A diferencia de la mayoría de las otras infecciones por protozoos, el diagnóstico rara vez se realiza mediante la detección o recuperación de organismos, sino que depende en gran medida de procedimientos serológicos. Los parásitos se pueden detectar en muestras de biopsia, células de la capa leucocitaria o líquido cefalorraquídeo. Sin embargo, la detección de taquizoitos en estos materiales puede resultar difícil. Estas muestras también pueden usarse para inocular ratones o células de cultivo de tejidos o analizarse mediante PCR. Sin embargo, los resultados pueden ser engañosos, ya que muchas personas han estado expuestas al Toxoplasma y albergan quistes en los tejidos (bradizoítos). Por lo tanto, las pruebas serológicas son un componente recomendado del diagnóstico.
El diagnóstico serológico de Toxoplasma también es complejo debido a la prevalencia de individuos seropositivos. Los títulos elevados de anticuerpos por sí solos no son evidencia definitiva de una infección aguda. Las infecciones congénitas son igualmente difíciles de diagnosticar serológicamente porque la IgG materna atraviesa la placenta y persiste durante varios meses. La evidencia de una infección aguda son títulos altos de IgM y/o aumentos significativos en los títulos de anticuerpos totales junto con los síntomas. Las técnicas de imagen (CT, MRI) también pueden ser útiles en el diagnóstico de la encefalitis toxoplásmica.
Indicaciones y duración del tratamiento :
- Los pacientes sintomáticos deben ser tratados hasta que las manifestaciones hayan remitido y haya evidencia de inmunidad adquirida.
- Los pacientes con retinocoroiditis deben recibir suplementos de corticosteroides para suprimir la inflamación.
- Las mujeres embarazadas deben recibir tratamiento con espiramicina para prevenir la infección del feto.
- Los recién nacidos deben recibir tratamiento durante 12 meses para evitar apariciones posteriores de retinocoroiditis.
- Los pacientes inmunocomprometidos deben recibir tratamiento. La terapia debe continuar durante 4 a 6 semanas después del cese de los síntomas, seguida de profilaxis mientras dure la inmunosupresión.
El tratamiento recomendado es la combinación sinérgica de pirimetamina más suplemento de sulfadiazina con ácido folínico (Leucovorin®).
| Prevención |
|---|
| carne crudacocine bien (66C, 150F)use guantes al manipularlavarse las manos después de manipularlavar tablas de cortar, encimeras, utensilios, etc.heces de gatoLimpiar la caja de arena rápidamente (<24 h).use guantes mientras hace jardineríalavarse las manos después de trabajar en el jardín o limpiar la caja de arenalavar y pelar frutas y verdurascubrir la caja de arenasiempre ten al gato en casacontrolar los perros callejerosno adquiera nuevos gatos durante el embarazo |
El pronóstico de la toxoplasmosis aguda en adultos inmunocompetentes es excelente. Las infecciones agudas en el feto o en los niños pequeños pueden ir seguidas de ataques repetidos de retinocoroiditis. El tratamiento parece reducir la frecuencia de estos ataques. Si se inicia lo suficientemente temprano, el tratamiento de pacientes inmunodeprimidos generalmente produce mejoras, pero los recrudescencias son comunes.
Las medidas de control de la toxoplasmosis se centran en evitar las dos principales fuentes de infección: la carne cruda y las heces de gato contaminadas. Las actividades preventivas (Cuadro) incluyen: evitar la ingestión de oocistos esporulados o quistes tisulares, destrucción de las formas infecciosas (p. ej., calentamiento) y prevención de la infección de las mascotas. La prevención es especialmente importante durante el embarazo, cuando las consecuencias de la infección son más graves.
Reseñas sobre Toxoplasma :
- Capítulo sobre Toxoplasma gondii por JP Dubey
- Tenter et al (2000) Int. J. Parasitol. 30, 1217
- D. Hill, JP Dubey (2002) Toxoplasma gondii : transmisión, diagnóstico y prevención. Microbiología clínica e infección 8:634-640 .
- DE Hill, S Chirukandotha y JP Dubey (2005) Biología y epidemiología de Toxoplasma gondii en el hombre y los animales. Reseñas de investigaciones sobre salud animal 6:41-61 .
- JG Montoya y O Liesenfeld (2004) Toxoplasmosis. The Lancet 363:1965-1976 .
| Neospora caninum |
|---|
| Neospora caninum está estrechamente relacionada con Toxoplasma gondii y exhibe una morfología casi idéntica. Al igual que Toxoplasma , Neospora infecta a muchos animales domésticos y es una de las principales causas de abortos y muertes fetales en el ganado bovino en todo el mundo. Los huéspedes definitivos son perros que presentan enfermedades neuromusculares. Los humanos no somos un huésped. Los perros se infectan después de la ingestión de tejidos infectados de huéspedes intermediarios. Los ovocitos no esporulados se eliminan en las heces y esporulan en el medio ambiente. Los huéspedes intermediarios adquieren la infección por ingestión de ooquistes esporulados. Sin embargo, a diferencia del Toxoplasma , los huéspedes intermediarios no pueden adquirir la infección mediante la ingestión de formas de tejido de otros huéspedes intermediarios. La infección puede transmitirse de forma congénita y el parásito se mantiene fácilmente en el ganado vacuno y en los perros mediante transmisión vertical. También se ha identificado un ciclo selvático que involucra venados de cola blanca y coyotes (Rosypal y Lindsay, Tr. Parasitol. 21, 349. 2005 ). |
Babesiosis
| Nota histórica |
|---|
| En 1893, Smith y Kilborne informaron que las garrapatas transmiten B. bigemina , la causa de la fiebre del ganado de Texas. Esta fue la primera demostración de una enfermedad transmitida por artrópodos y probablemente inspiró el descubrimiento posterior de otras enfermedades transmitidas por vectores, como la fiebre amarilla y la malaria. |
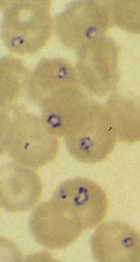
La babesiosis es una rara infección zoonótica transmitida por garrapatas. Los agentes etiológicos, especie Babesia , son parásitos sanguíneos que infectan a una amplia variedad de animales domésticos y salvajes en todo el mundo. Babesia y Theileria forman un grupo llamado piroplasmas, en referencia a las formas intraeritrocíticas que en algunas especies tienen forma de pera. Los piroplasmas causan enormes pérdidas de ganado en zonas endémicas. Se ha especulado que la plaga del ganado egipcio descrita en el libro bíblico del Éxodo pudo haber sido la fiebre del agua roja causada por B. bovis .
Los dos géneros de piroplasma generalmente se distinguen por la falta de un ciclo preeritrocítico en Babesia y la falta de transmisión transovárica en Theileria (ver ciclo de vida a continuación). Los datos moleculares indican que las especies de Babesia y Theileria no forman grupos monofilógenos respectivos. En particular, muchas especies de Babesia , que habían sido agrupadas informalmente como Babesia “pequeña” , están más estrechamente relacionadas con Theileria . De acuerdo con estos datos moleculares, ninguna Babesia pequeña (a diferencia de la Babesia “grande” ) parece transmitirse transováriamente en las garrapatas, lo que sugiere la necesidad de reevaluar la clasificación del piroplasma. (Ver G Uilenberg, 2006, Babesia – Una descripción histórica, Veterinary Parasitology 138, 3-10 .)
| Babesiosis humana |
|---|
| EspeciesUbicaciónAnfitrión del reservorioVectorCasosMortalidadB. microtiEstados Unidosratones de campo y topillos*Ixodes escapular>20005%B. duncaniEstados Unidos?¿ Ixodes pacífico?911 %B. divergentesEuropabovinos y otros rumiantesIxodes ricinus>3050%* Peromyscus leucopus (ratón de patas blancas) y Microtus pennsylvannicus , respectivamente. |
Se ha informado que muchas especies de Babesia infectan a los humanos. Las tres especies más predominantes que infectan a los humanos son B. microti, B. duncani y B. divergens (Tabla). Las infecciones por otras especies han sido poco documentadas o se han limitado a unos pocos casos aislados. Los casos iniciales se asociaron con esplenectomía u otras condiciones inmunocomprometidas. Sin embargo, se han descrito personas inmunocompetentes infectadas por Babesia y que no presentan síntomas clínicos. Además, las encuestas serológicas sugieren que la infección puede estar infradiagnosticada. El mayor foco de infecciones humanas en Estados Unidos se ha producido en la región costera nororiental, lo que dio origen al nombre de fiebre de Nantucket, y en la parte superior del medio oeste. La infección en Europa es aparentemente más rara que en Estados Unidos, pero más mortal. La mayoría de estas infecciones se han asociado con personas que tienen contacto frecuente con el ganado.
Ciclo vital
Babesia exhibe un ciclo de vida típico apicomplejo caracterizado por merogonía, gametogonía y esporogonia (Figura). La infección es adquirida por el huésped vertebrado cuando los esporozoítos (Sp) se transfieren durante la alimentación de la garrapata. Los esporozoitos invaden los eritrocitos utilizando un mecanismo de invasión similar al de otros Apicomplexa. (Ver discusión detallada sobre la invasión de las células huésped por el parásito de la malaria ). A diferencia de Plasmodium , la membrana vacuolar parasitófora (PVM) se desintegra después de la invasión y el parásito está en contacto directo con el citoplasma de los eritrocitos del huésped. Los trofozoitos (Tr) se dividen por fisión binaria y producen merozoitos (Mz), que infectan eritrocitos adicionales y reinician el ciclo replicativo. En algunas especies, ocasionalmente se observa una tétrada, denominada cruz de Malta.
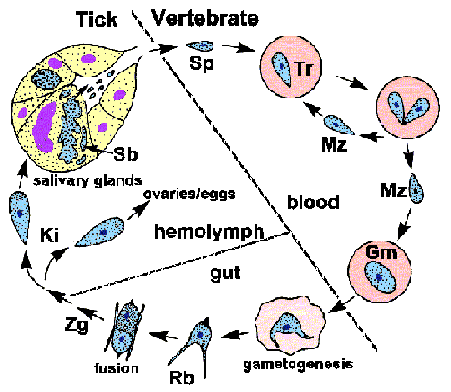
Algunos de los trofozoítos se convertirán en gametocitos (Gm) o gamonts, que son responsables de iniciar la infección en la garrapata vectora. Los gametocitos sufren cambios morfológicos dentro del intestino de la garrapata y se convierten en cuerpos de rayos (Rb; también conocido como Strahlenkörper). Dos cuerpos de rayos (es decir, gametos) se fusionarán para formar un cigoto (Zg) que luego se desarrollará en un cineto (Ki). El cinete penetra la membrana peritrófica y el epitelio intestinal para acceder a la hemolinfa. Las Babesia grandes , como B. divergens y B. canis , son capaces de invadir varios órganos y sufrir una mayor replicación. Lo más notable es la invasión de los ovarios y los óvulos que conduce a una transmisión transovárica a la descendencia de la garrapata.
La esporogonia se inicia cuando los cinetes invaden las glándulas salivales. El parásito se expande y llena una célula huésped hipertrofiada y se convierte en un esporoblasto multinucleado (Sb; también conocido como esporonto). Los esporozoitos maduros, que poseen orgánulos apicales, brotarán de este esporoblasto indiferenciado cuando la garrapata se alimente nuevamente de un nuevo huésped. Un solo esporoblasto puede producir entre cinco y diez mil esporozoítos. Luego, los esporozoitos se inyectarán en el huésped con la saliva, completando así el ciclo de vida.
| Theileria y linfoblastogénesis |
|---|
| Las especies de Theileria infectan y causan enfermedades en el ganado, y especialmente en el ganado, en muchas partes del mundo. La más grave es la fiebre del ganado bovino de la costa este, causada por T. parva . Tiene una mortalidad del 90 al 100 por ciento en África. T. annulata causa una enfermedad más leve en el ganado bovino a lo largo del Mediterráneo y en el Medio Oriente conocida como teileriosis tropical. Theileria está estrechamente relacionada con Babesia y exhibe un ciclo de vida muy similar (Figura 16.1). La principal diferencia es una etapa preeritrocítica exhibida por especies de Theileria . Aunque se sospecha dicha etapa preeritrocítica en B. microti . Los esporozoitos invaden los linfocitos e inducen la proliferación de los linfocitos del huésped mediante un mecanismo desconocido. El parásito se convierte en un esquizonte multinucleado (es decir, meronte) que se divide coincidiendo con la replicación del linfocito en proliferación y, por tanto, se transfiere un esquizonte a cada uno de los linfocitos hijos. Los merozoitos resultantes invaden los eritrocitos y finalmente se convierten en gamontes que son infecciosos para la garrapata. Es el proceso linfoproliferativo el que conduce a las manifestaciones graves de la enfermedad asociadas con las teileriosis. Esta transformación de linfocitos es reversible porque el tratamiento conduce a la eliminación del parásito y se inhibe la posterior proliferación de linfocitos. |
Características clínicas
En personas con bazo intacto, la infección generalmente desaparece espontáneamente y se caracteriza por una aparición gradual de malestar, fiebre, dolor de cabeza, escalofríos, sudoración, mialgia, fatiga y debilidad. Una anemia hemolítica de leve a moderada también puede acompañar a estos síntomas. Muchas de las infecciones se resolverán por sí solas sin tratamiento, pero los parásitos pueden persistir durante meses. La enfermedad tiende a ser más fulminante y grave en personas esplenectomizadas o inmunodeprimidas y puede poner en peligro la vida. Pueden ocurrir parasitemias >25% y anemia grave.
No existen fármacos claramente eficaces contra la babesiosis. El tratamiento recomendado es clindamicina + quinina. También se ha demostrado que la pentamidina suprime, pero no elimina, la parasitemia. La cloroquina, aunque no parece afectar la parasitemia, sí proporciona cierto alivio sintomático, que puede deberse a sus propiedades antiinflamatorias. Se ha demostrado que atovacuona + azitromicina es tan eficaz como clindamicina + quinina, pero con menos efectos adversos (Krause et al, 2000, N. Engl. J. Med 343:1454). La exanguinotransfusión se ha utilizado como una medida para salvar vidas en pacientes gravemente enfermos.
Revisión sobre babesiosis:
- Vannier E y Krause PJ (2012) Babesiosis humana. NEJM 366:23972407 .

I’ve always been captivated by the wonders of science, particularly the intricate workings of the human mind. With a degree in psychology under my belt, I’ve delved deep into the realms of cognition, behavior, and everything in between. Pouring over academic papers and research studies has become somewhat of a passion of mine – there’s just something exhilarating about uncovering new insights and perspectives.